Proceso de Selección de Medicamentos y Dispositivos Médicos
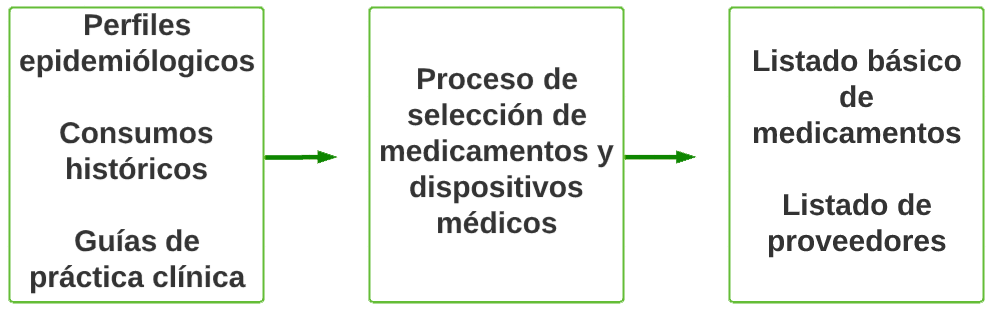
El proceso de selección de medicamentos y dispositivos médicos, bajo criterios técnico-científicos define el Listado Básico de Medicamentos y Dispositivos Médicos (LBMDM), el cual contiene los medicamentos y dispositivos médicos con los que se deben contar en una institución para atender las principales necesidades en salud de un contexto específico (población), garantizando su acceso oportuno. Estos medicamentos y dispositivos médicos definidos en el LBMDM, deben ser seleccionados con base en aspectos de necesidad, pertinencia, disponibilidad, seguridad, eficacia, costo-efectividad.
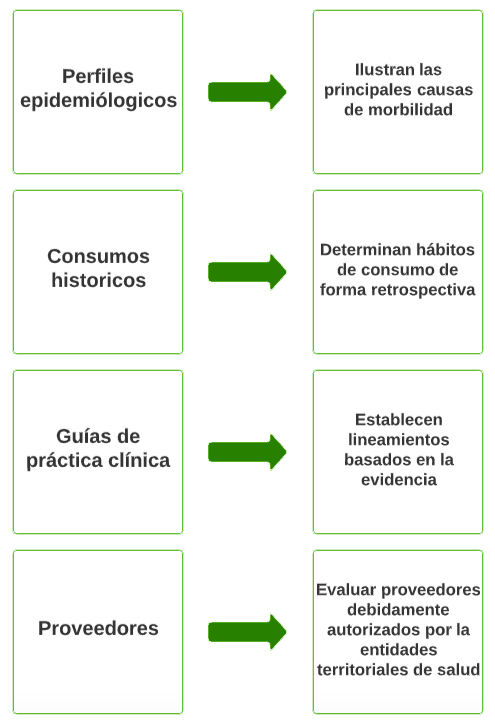
Para ello se requiere de información relacionada con:
El LBMDM se diferencia del inventario en cuanto no se limita a un listado de referencias o ítems con cantidades. Se recomienda ser revisado y actualizado, anualmente. La Resolución 3100 de 2019, establece que este listado debe al menos contener la siguiente información:
Información mínima en el LBMDM para Medicamentos:
- • Principio activo.
- • Forma farmacéutica.
- • Concentración.
- • Lote.
- • Fecha de vencimiento.
- • Presentación comercial.
- • Unidad de medida.
- • Registro sanitario vigente o permiso cuando se autorice, expedido por el INVIMA.
Información mínima en el LBMDM para Dispositivos Médicos:
- • Descripción.
- • Marca del dispositivo.
- • Serie (cuando aplique).
- • Presentación comercial.
- • Registro sanitario vigente o permiso de comercialización expedido por el INVIMA.
- • Clasificación por riesgo (información consignada en el registro sanitario o permiso de comercialización).
- • Vida útil, cuando aplique.
- • Lote.
- • Fecha de vencimiento.
Por su parte, el listado de proveedores debe ser evaluado y actualizado periódicamente en función de los resultados de las evaluaciones de desempeño de estos.
